A data representa o penû¤ltimo dia do prazo de dez dias estabelecido para anûÀlise
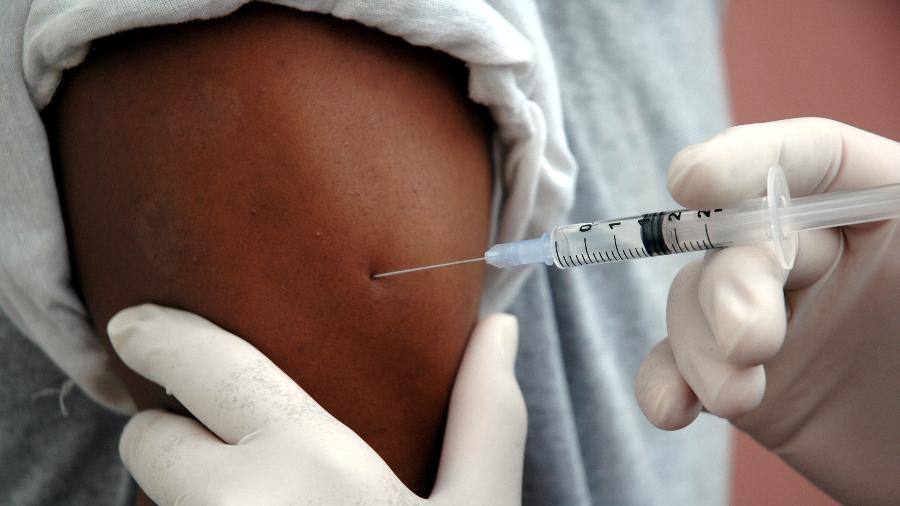
A Anvisa (Agûˆncia Nacional de Vigilância SanitûÀria) informou que estûÀ prevista para o próximo domingo (17) a decisão da diretoria colegiada do órgão sobre os pedidos de autorização emergencial das vacinas contra o novo coronavûÙrus.
Foram submetidas para anûÀlise na û¤ltima sexta-feira (8) a CoronaVac, do Instituto Butantan em parceria com o laboratório Sinovac, e a da Fiocruz (Fundação Oswaldo Cruz), em parceria com a Universidade de Oxford e o laboratório AstraZeneca.
A data representa o penû¤ltimo dia do prazo de dez dias estabelecido para anûÀlise. "Para tanto, faz-se necessûÀria a entrega, em tempo hûÀbil para anûÀlise, dos documentos faltantes e complementares", afirma a Anvisa em nota.
O Instituto Butantan jûÀ começou a enviar os documentos pendentes sobre os dados da CoronaVac para a Anvisa (Agûˆncia Nacional de Vigilância SanitûÀria). O status do relatório, atualizado às 16h17 de hoje, indica que 37,64% dos registros ainda precisam de complementação. Em anûÀlise são 16,19%.
O processo total para regularizar o pedido emergencial da vacina estûÀ 40,07% concluûÙdo. De acordo com a Anvisa, 5,47% dos estudos não foram apresentados ainda pelo Butantan — o que inclui o relatório de imunogenicidade, que é a capacidade de uma substância provocar uma resposta imune.
O governo paulista precisa da autorização da Anvisa para realizar seu plano estadual de imunização, cuja primeira fase estûÀ prevista para começar no próximo dia 25.
Após divulgar taxas de eficûÀcia parciais da CoronaVac de 78% na semana passada, o Governo de São Paulo revelou hoje que a eficûÀcia geral da vacina, que engloba todos os grupos analisados nos testes clûÙnicos, é de 50,38%. O resultado era muito aguardado para avaliar de forma mais completa a vacina contra a covid-19 do Instituto Butantan em parceria com o laboratório chinûˆs Sinovac.
O nû¤mero jûÀ era esperado, como antecipou o UOL ontem, numa previsão de que a eficûÀcia geral ficasse entre 50% e 60%. Como o mûÙnimo exigido para a aprovação pela Anvisa (Agûˆncia Nacional de Vigilância SanitûÀria) é de 50%, o nû¤mero de 50,38% estûÀ dentro do aceitûÀvel e também atende aos padrões da OMS (Organização Mundial da Saû¤de). Os pesquisadores afirmam que 0,3% dos voluntûÀrios apresentaram reações alérgicas e não foram registrados efeitos adversos mais graves.
Em relação à vacina da Fiocruz/AsrtraZeneca, a Anvisa informa que 14,44% dos registros ainda precisam de complementação. Em anûÀlise estão 53,17%, e o processo total para regularizar o pedido emergencial da vacina estûÀ 32,39% concluûÙdo.